摘要:
在使用雄激素受体(AR)通路抑制剂治疗后,20%的前列腺癌患者通过摆脱AR依赖而进展。这些肿瘤经历表观遗传学重编程,将去势抗性前列腺癌腺癌(CRPC-Adeno)转化为神经内分泌前列腺癌(CRPC-NEPC)。目前还没有针对CRPC-NEPCs的靶向治疗方法,而且有最小的类器官模型来发现针对这些侵袭性肿瘤的新治疗靶点。在这里,结合患者肿瘤蛋白质组学、RNA测序、空间组学和合成水凝胶类器官,定义了调节CRPC-NEPCs表型的细胞外基质(表观遗传基础。肿瘤表达的ECM的短期培养可差异调控CRPC-NEPCs中的DNA甲基化和动员基因。ECM类型明显调控对表观遗传靶点的小分子抑制剂和多巴胺受体D2(DRD2)的反应,后者是神经内分泌肿瘤中未得到充分研究的靶点。在免疫缺陷小鼠体内,用抑制剂治疗DRD2时显示出强烈的抗肿瘤反应。最后,我们证明了在耐药ECM条件下,CRPCNEPCs的治疗反应可以通过首先使用表观遗传抑制剂进行细胞重编程,然后进行DRD2治疗来克服。合成的类器官表明了ECM在CRPC-NEPCs中对靶向治疗的治疗反应中的调节作用,并使发现克服耐药性的疗法成为可能。

介绍
在这里,作者对111名患者进行了转录组分析,并结合了蛋白质组学、空间组学和对患者活检的显微镜分析等专业技术,以确定CRPC-Adeno和CRPC-NEPC中的ECM和相关微环境。根据这些发现,我们开发了一种基于合成聚合物的马来酰亚胺官能化聚(乙二醇)(PEG-4MAL)水凝胶平台,用于在定义的ECM微环境下培养CRPC-Adeno和CRPC-NEPC患者肿瘤细胞。我们研究了仿生合成ECM对肿瘤形态、肌动蛋白细胞骨架以及与CRPC-NEPC进展相关的转录组和表观遗传特征变化的影响。我们在CRPC-NEPCs中证明了ECM依赖性EZH2i反应,其中耐药性可以通过EZH2i的细胞重编程来克服,然后用神经内分泌靶向实验疗法进行治疗。呈现ECM特异性生物粘附配体的合成水凝胶平台可以为Matrigel目前无法提供的CRPC-Adeno或CRPC-NEPC提供更明确的微环境,随后调节转录组和表观遗传学,并能够发现新的单一和组合疗法。
方法与结果
ECM-整合素粘附受体相互作用提供了调节癌细胞的细胞和分子命运的关键信号,包括存活、基因表达和转移能力。ECM-整合素相互作用也可以通过机械转导影响染色质状态。本研究实验结果显示,CRPC-Adeno患者肿瘤表现出细胞粘附蛋白的高表达;CRPC-Adeno和CRPC-NEPC患者肿瘤表现出相似的生物粘附微环境;CRPC-NEPCMatrigel类器官表达的整合素水平与CRPC-Adeno类器官不同(见图一);基于合成水凝胶的前列腺癌类器官中定义的ECM调节患者衍生细胞的表型和形态(见图二);PEG-4MAL类器官中的ECM调节表观遗传调节因子EZH2的表达和对EZH2i的反应(见图三);基于PEG-4MAL水凝胶的类器官的ECM成分调节CRPC-NEPCs的DNA甲基化谱;基于PEG-4MAL水凝胶的类器官的ECM组成调节CRPC-Adeno和CRPC-NEPCs的基因动员(见图四);ECM差异调节CRPC-NEPCs中的基因表达途径(见图五);多巴胺受体D2(DRD2)作为CRPC-NEPCs的新疗法(见图六、图七)。
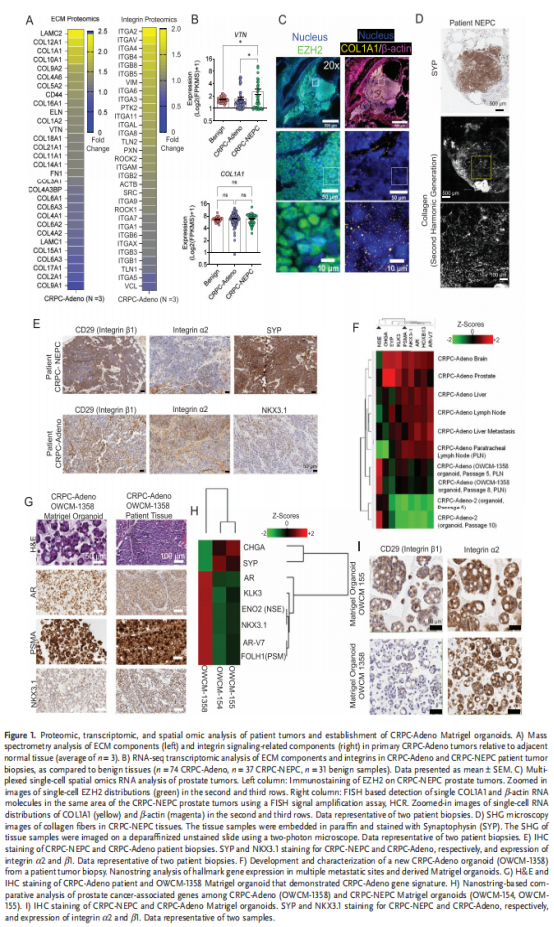
(图一)
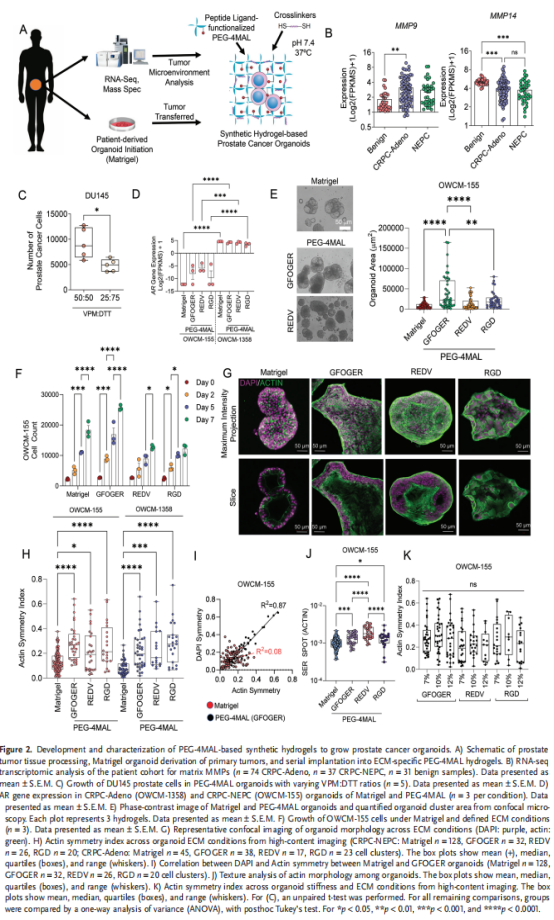
(图二)
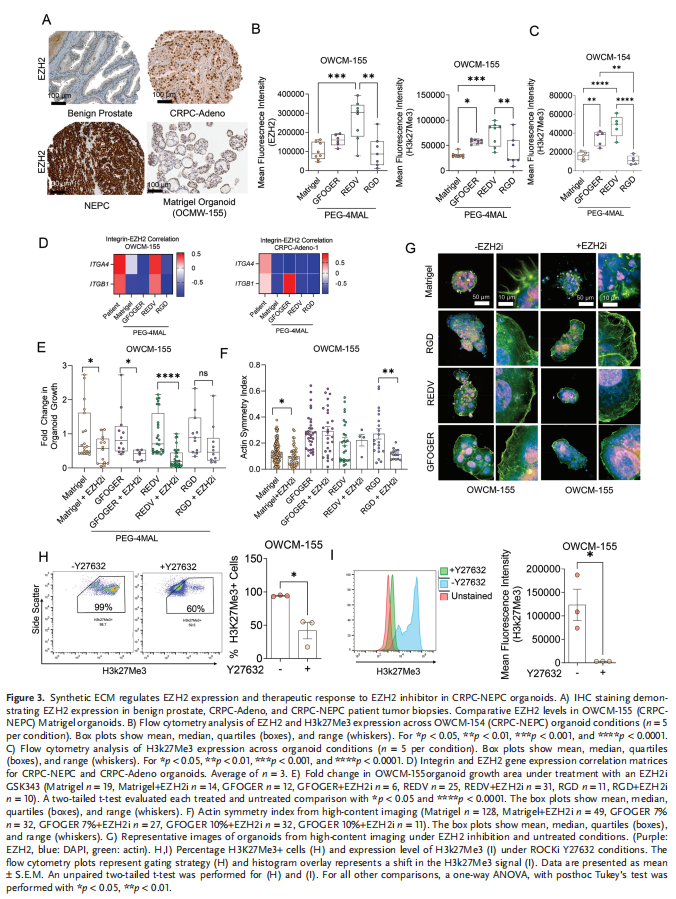
(图三)

(图四)
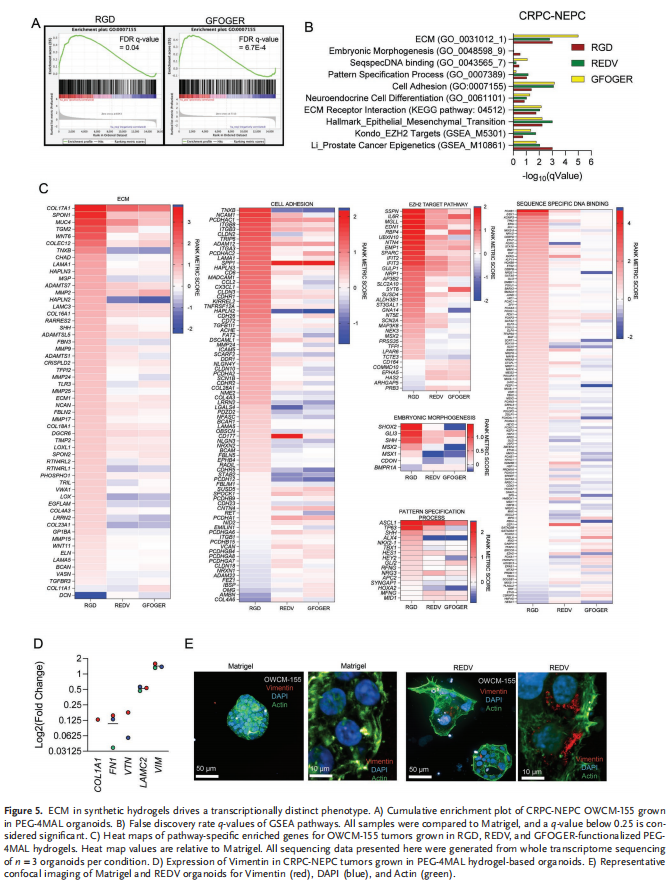
(图五)
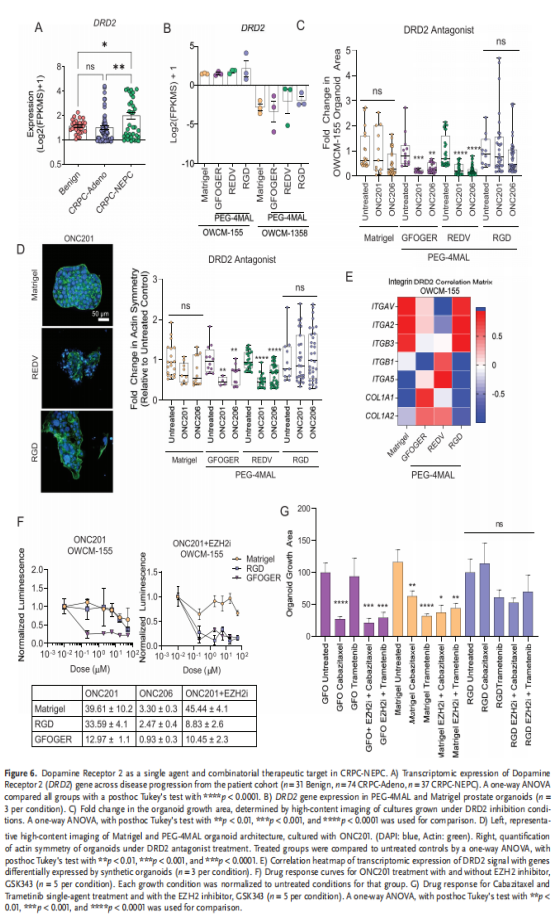
(图六)
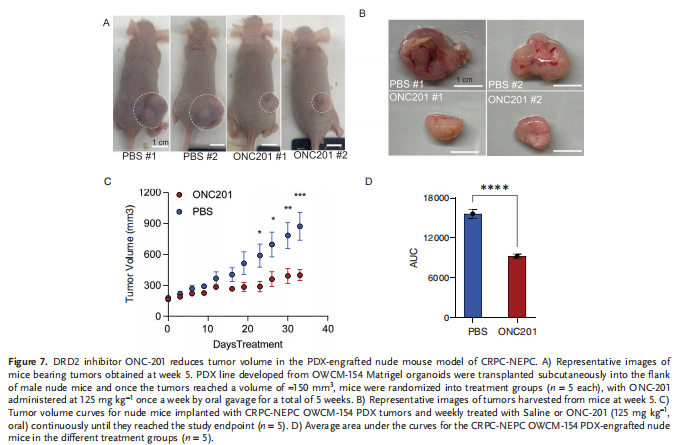
(图七)
结论
CRPC-NEPC肿瘤研究的一个主要障碍是缺乏现有的临床前模型,并且CRPC-NEPC类器官很少存在。在这项工作中,我们设计了基于合成水凝胶的ECM来生长CRPC-NEPC和CRPC-Adeno类器官。合成ECM的生物启发来自患者肿瘤组织蛋白质组学、空间组学、免疫组织化学和转录组学数据。与Matrigel相比,我们证明生物工程ECM调节CRPC-NEPC中的生长、EZH2表达及其活性、DNA甲基化状态并动员不同的基因,这可能与治疗药物反应的差异相关。这些发现表明,不同的ECM成分可以差异调节基因表达和DNA甲基化。使用这些合成的PEG-4MAL水凝胶生长的类器官,我们已经确定了一个潜在的治疗靶点,DRD2抑制剂ONC-201,用于CRPC-NEPC,并阐明了ECM-整合素相互作用如何使这些肿瘤对EZH2和DRD2拮抗剂活性敏感。我们预计这项工作将激发未来研究ECM特异性TME中长期反应的努力,并结合其他基于细胞的因素,包括癌症相关的成纤维细胞、免疫细胞和基质细胞。我们进一步预计PEG-4MAL类器官将提高从患者原发性肿瘤中提取患者类器官的成功率,目前使用Matrigel的成功率保持在16%(4/25)。我们预计这项工作将激发未来研究ECM特异性TME中长期反应的努力,并结合其他基于细胞的因素,包括癌症相关的成纤维细胞、免疫细胞和基质细胞。我们进一步预计PEG-4MAL类器官将提高从患者原发性肿瘤中提取患者类器官的成功率,目前使用Matrigel的成功率保持在16%(4/25)。我们预计这项工作将激发未来研究ECM特异性TME中长期反应的努力,并结合其他基于细胞的因素,包括癌症相关的成纤维细胞、免疫细胞和基质细胞。我们进一步预计PEG-4MAL类器官将提高从患者原发性肿瘤中提取患者类器官的成功率,目前使用Matrigel的成功率保持在16%(4/25)。

