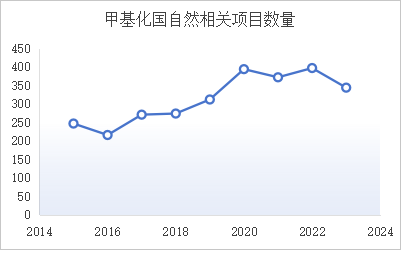
为辅助大家进行课题选题及国自然基金撰写,熟悉最新研究热点及进展,尤其是协助找到最新的课题,我们陆续对国自然的热点进行了部分解析。今天我们通过一篇研究,详细了解一下有关“蛋白甲基化”这一科研热点。
「原理」
蛋白的甲基化(methylation)是指将甲基酶促转移到蛋白质的某个残基上,通常是赖氨酸或精氨酸,也包括组氨酸、半胱氨酸和天冬酰胺等。甲基化通过调控基因表达、表观遗传、代谢、信号传导及免疫应答,影响细胞功能。异常的调控修饰会导致功能异常,进而导致多种疾病的发生,如肿瘤、神经退行性疾病和心血管疾病等。
「组蛋白甲基化制」
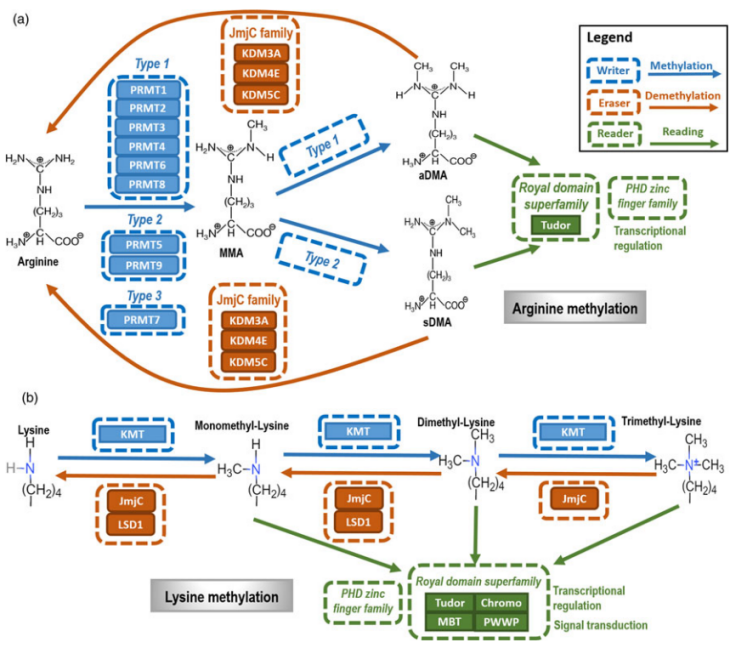
(a)精氨酸甲基化由PRMT催化甲基从SAM转移到精氨酸胍基团的氮原子(N)。
(b)赖氨酸甲基化是由KMT触发赖氨酸的单甲基化、二甲基化和三甲基化。
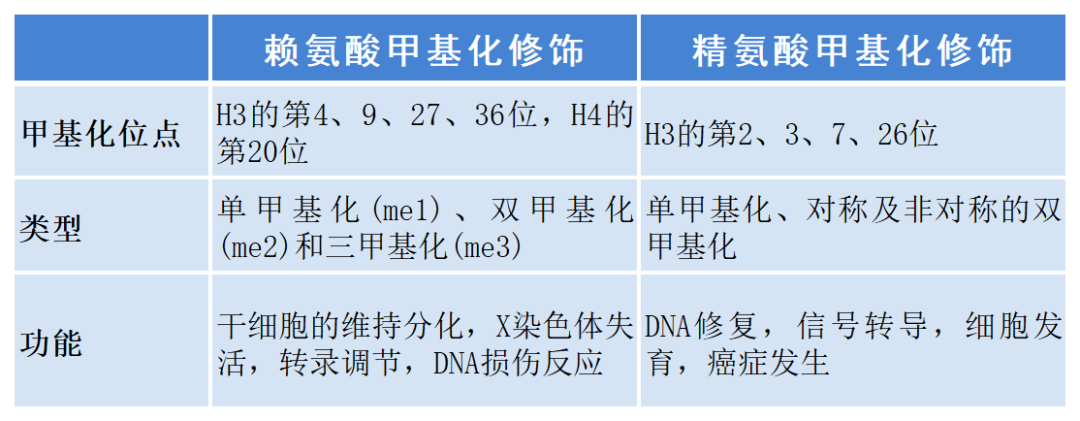
下表总结了组蛋白的精氨酸和赖氨酸甲基化发生的位点、类型、参与的甲基转移酶,以及甲基化修饰的作用和功能。
「研究方法」
揭秘蛋白质甲基化:五大生物技术手段
在蛋白甲基化研究中,常见研究方法主要包括WB,质谱,IP,Elisa,和FRET这5种,为了直观清晰地了解这5种方法在研究组蛋白甲基化中的优缺点,特整理了以下表格以供参考。

从以上表格不难看出,蛋白甲基化研究常见的5种方法中,每一种技术都有其独特的优势和局限性,在实际应用中,通常会根据研究目的、样品类型以及实验条件等多种因素综合使用这些技术,以获得更全面、准确的信息。
「高分文献解读」
文献1:
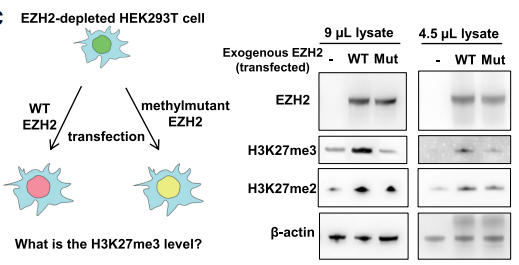
体外甲基化--EZH2的自动甲基化对于新生H3K27me3沉积至关重要实验将野生型(WT)或甲基突变型(Mut)EZH2质粒转染到EZH2耗尽的HEK293T菌株中。结果表明,在EZH2耗尽的菌株中,H3K27me3的丢失被WT EZH2挽救,但不能被甲基化突变体EZH2挽救[2]。
文献2:
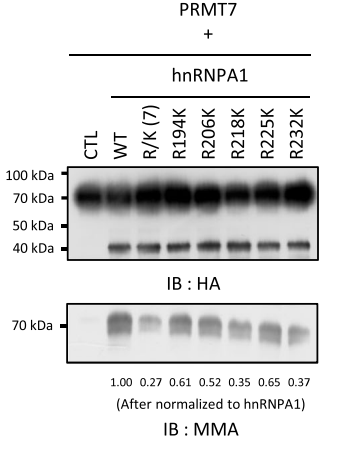
体外甲基化实验---hnRNPA1中的五个精氨酸甲基化位点受到PRMT7调控。
通过构建hnRNPA1每个位点(R194K、R206K、R218K、R225K和R232K)或全部五个精氨酸位点被赖氨酸替换(R/K (7))的突变体,将纯化的PRMT7蛋白与hnRNPA1(野生型)或突变体混合进行体外甲基化实验。结果发现单一位点突变减弱了PRMT7介导的甲基化,而所有五个精氨酸位点被替换的突变体具有 最显著的减弱效果,表明PRMT7在hnRNPA1中调控的五个精氨酸位点可以在体外得到验证。[3]
「国自然相关预实验」
1.临床样本检测及甲基化相关蛋白筛选:通过分析患者组织或体液样本,验证甲基化蛋白质的表达与患者预后或治疗反应的相关性。
2.甲基化相关检测:细胞或动物模型检测甲基化蛋白水平及甲基化相关指标的变化。
3.生信筛选与质谱联用:预测其相互作用蛋白或基因及蛋白甲基化精确位点的初步预测。
「国自然中标项目分享」
近几年国自然中标项目节选:
1、衣康酸调节组蛋白去甲基化酶JMJDIC介导巨噬细胞训练免疫在糖尿病肾脏病中的作用与机制研究
2、组蛋白去甲基化酶OsJMJ704调控水稻耐盐性的分子机制研究
3、Nr 4a1的甲基化修饰调控IDH1 在慢性应激所致颗粒细胞衰老中的作用及机制研究
4、KDM6A促进Tkt去甲基化改善新生小鼠缺氧缺血性神经元损伤的作用及机制研究
5、AHRR去甲基化调控棕色脂肪活化/脂肪棕色化减轻肥胖相关心肌纤维化的机制研究
【参考文献】
[1] Dai X, Ren T, Zhang Y, et al. Methylation multiplicity and its clinical values in cancer[J]. Expert Reviews in Molecular Medicine, 2021, 23: e2.
[2] Wang X, Long Y, Paucek R D, et al. Regulation of histone methylation by automethylation of PRC2[J]. Genes & Development, 2019, 33(19-20): 1416-1427.
[3] Li W J, He Y H, Yang J J, et al. Profiling PRMT methylome reveals roles of hnRNPA1 arginine methylation in RNA splicing and cell growth[J]. Nature Communications, 2021, 12(1): 1946.
科研实验外包 想了解更多请关注:https://www.do-gene.cn

