回顾前面3种lncRNA发挥功能的方式,我们可以发现lncRNA主要扮演一个间接促进者的作用,通过与功能蛋白结合,增强功能蛋白对下游靶蛋白的调控。而最后,我们来看看lncRNA是如何直接调控靶蛋白的表达。
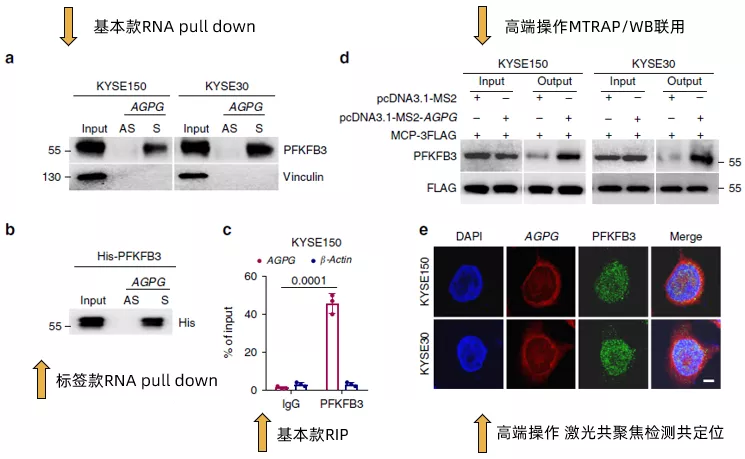
这篇范文2020发表于大家所熟知的nature communication,虽然该杂志一直有些争议,但是我们还是可以默默地感受一下贫富差距。作者首先说明了在之前的研究中通过RNA pull down联用质谱的方式确认了lncRNA AGPG与靶蛋白PFKFB3的结合(没错,就是在lncRNA与RBP中提到的方法),然后在本文中通过RNA pull down(Fig3a,Fig3b)以及RIP(Fig3c)做了进一步的验证。
值得注意的是,在Fig3b中作者还加入了包含His标签的重组型外源PFKFB3的验证。进一步地,作者使用了在之前几篇文章中都没有出现过的MTRAP/WB联用(Fig3d)以及FISH/免疫荧光激光共聚焦共定位(Fig3e)的方法,再次验证了AGPG与PFKFB3的结合。
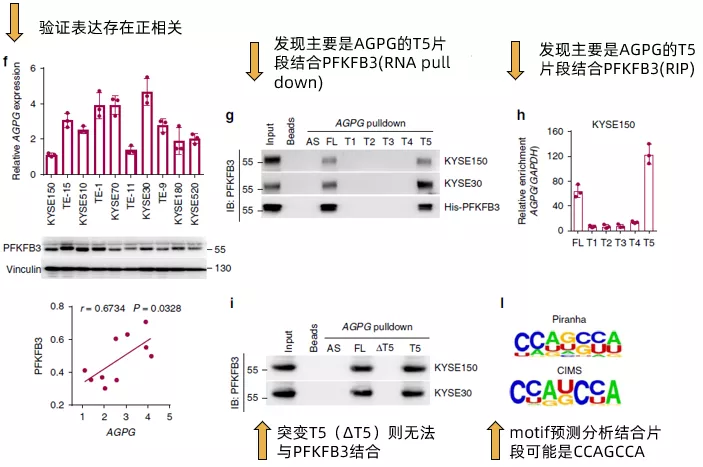
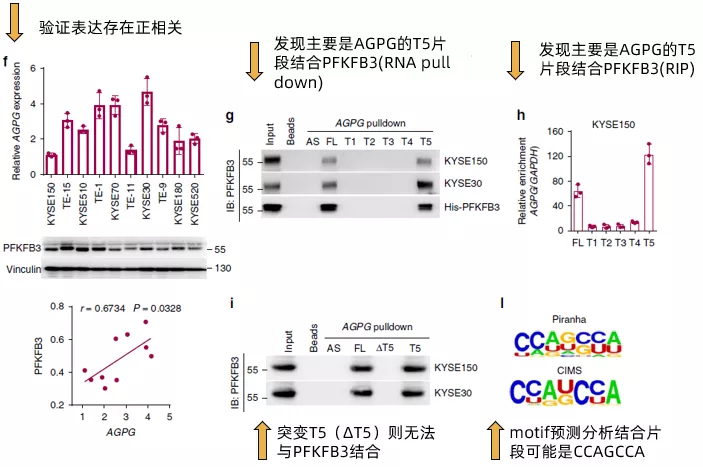
接下来,作者在多种食管鳞状细胞癌细胞系以及临床组织样本中确认了AGPG与PFKFB3的表达呈现正相关(Fig3f),且其在补充材料的数据甚至做到了拷贝数和分子数的绝对值的对应关系(~ 400–700 AGPG molecules per cell versus ~4400–7400 PFKFB3 molecules per cell)。通过计算机分析AGPG的二级结构,发现其有5个主要的branches(还是放在了补充材料里),通过合成全长以及这五个branches片段(T1~T5)的AGPG,作者发现T5片段是主要结合PFKFB3的区域(Fig 3g,Fig 3h)。而突变T5(ΔT5)则无法与PFKFB3结合。最后,通过motif预测分析,发现结合PFKFB3的片段可能是CCAGCCA(Fig 3I)。简单来看,fig3的所有这些结果,其实就是说明了AGPG与PFKFB3的结合并影响了PFKFB3的表达,但是在设计上充分展示了丰度(经费)。
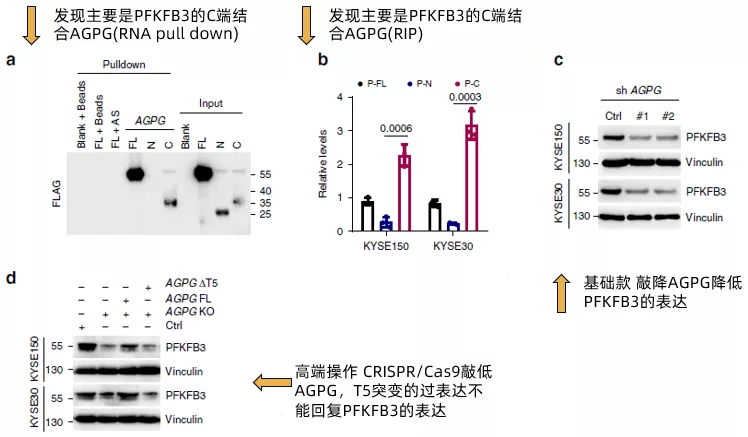
在确认了AGPG的T5片段能够与PFKFB3结合后,作者进一步将PFKFB3拆分为全长,N端和C端,通过RNA pull down(fig4a)和RIP(fig4b)证实了PFKFB3通过C端与AGPG结合。然后,作者评估了AGPG对PFKFB3的表达的影响。AGPG沉默明显降低PGKFB3的表达(fig4c),使用CRISPR / Cas9的CRISPR KO细胞得到了类似的结果(fig4d)。而AGPG的T5突变(ΔT5) 未能回复PFKFB3的表达。
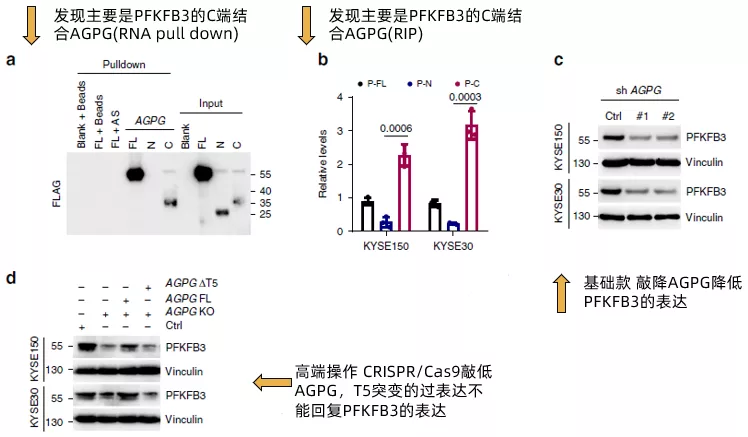

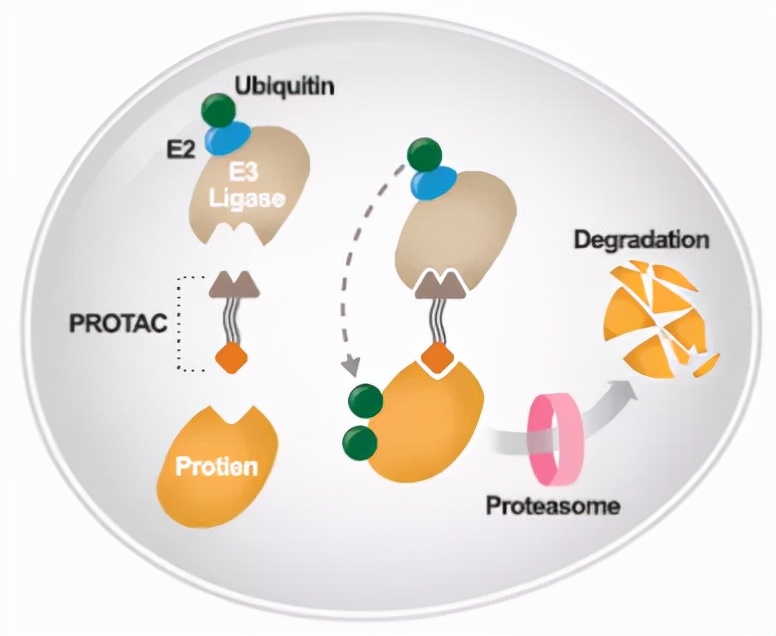
接下来到了关键的部分,作者援引文献说明PFKFB3经常经由泛素化(polyubiquitination)修饰的方式受到蛋白酶体(proteosomal degradation)的降解。在这里我们插播一段关于泛素化和蛋白降解的基本原理的描述:
E1泛素激活酶(ubiquitin-activating enzyme), E2泛素偶联酶(ubiquitin-conjugating enzymes), E3泛素连接酶(E3 ubiquitin ligase)通过给蛋白的赖氨酸残基(K)加上泛素化标签(ubiquitin),导致被修饰的蛋白将进入蛋白酶体中被降解。这是细胞降解蛋白的主要方式。其中,研究最广的是E3 ligase。
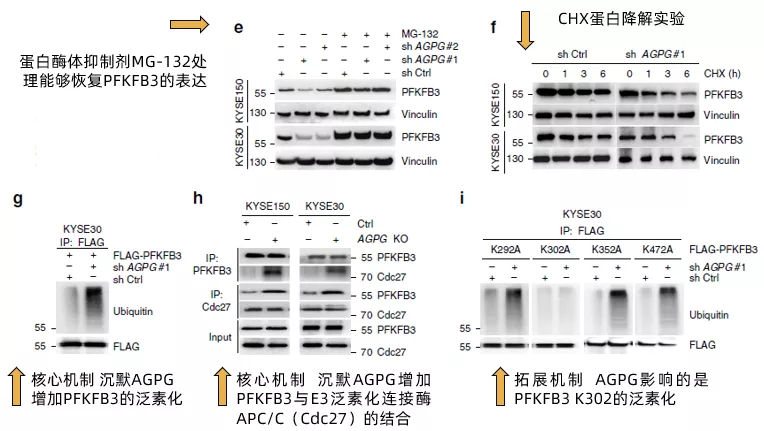
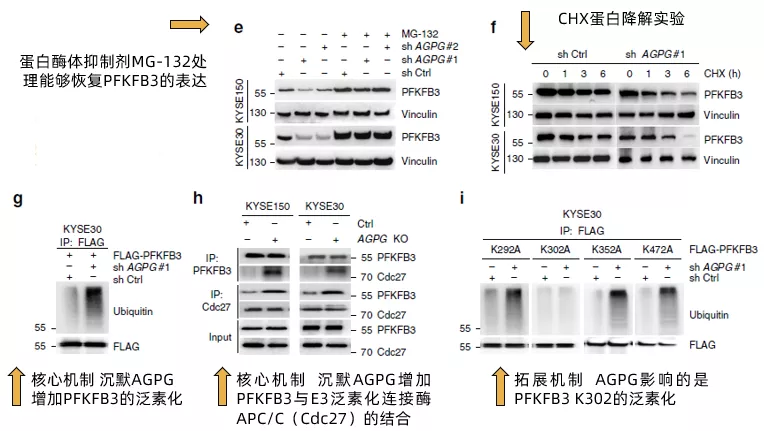
回到文中,作者发现蛋白酶体抑制剂MG-132能够恢复PFKFB3的表达(fig4e),暗示APGP沉默引起的PFKFB3的降低与蛋白酶体降解有关;且通过CHX蛋白降解实验验证了沉默AGPG会加速PFKFB3的降解(Fig 4f)。接下来,通过检测蛋白的泛素化,作者发现沉默AGPG会大幅增加PFKFB3蛋白的泛素化水平(Fig 4g),增加PFKFB3与E3泛素连接酶APC/C的结合(Fig 4h),至于图中为什么用的是Cdc27,作者也给出了解释“active APC/C could be immunoprecipitated from cells using a monoclonal Cdc27 antibody”。
最后,作者进一步确认了AGPG通过影响PFKFB3 C端的某一个赖氨酸残基来避免其受到泛素化修饰。通过将C端四个赖氨酸(K)残基分别突变成丙氨酸(A),作者发现只有第302位的K突变后(K302A),PFKFB3不再被AGPG沉默升高,证实AGPG影响的是PFKFB3 K302的泛素化(Fig 4i)。至此,作者完成了AGPG通过结合PFKFB3,减少PFKFB3的泛素化,从而升高PFKFB3的稳定性的论证。
由于本文对机制的研究较深,我们尽量在去除一些高端超纲操作的情况下,总结一个亲民版的套路:
通过质谱或者预测,找到一个能够与lncRNA结合的蛋白,这个蛋白最好有报道被泛素化降解。通过RIP和RNA pull down验证其结合,通过WB,蛋白降解实验,验证lncRNA能够提高蛋白的稳定性,通过检测泛素化水平,以及CO-IP实验,验证lncRNA能够通过减少靶蛋白与E3泛素化连接酶的结合,从而减少靶蛋白的泛素化。

